Los materiales aislantes son materiales que presentan gran resistencia a que las cargas que lo forman se desplacen y los conductores tienen cargas libres y que pueden moverse con facilidad.




 Imagen de una autoclave (maquina que lleva acabo la esterilización a través del vapor de agua)
Imagen de una autoclave (maquina que lleva acabo la esterilización a través del vapor de agua)

 Ejemplo de un espectro de luz de una llama de alcohol.
Ejemplo de un espectro de luz de una llama de alcohol.

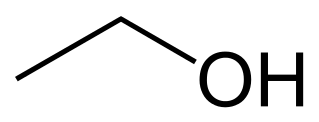
 |
| http://www.ucm.es/BUCM/media/images/blogs/fotoblog3502.jpg |

 |
| https://www.google.es/search?q=grupo+funcional&biw=1280&bih=699&source=lnms&tbm=isch&sa=X&ved=0ahUKEwi67Jz84YbLAhVFtxQKHZj4B7IQ_AUIBigB&dpr=1#imgrc=JQz4pqFHs9fOOM%3A |
 |
| https://www.google.es/search?q=carbono+asimetrico&biw=1280&bih=699&source=lnms&tbm=isch &sa=X&ved=0ahUKEwjz4erV3obLAhUHlxoKHcAWCJIQ_AUIBigB#imgrc=w5x9RKdMeCBgtM%3A |
 |
| AMBOS DE FÓRMULA MOLECULAR C5H12. SON ISÓMEROS DE CADENA. fuente: http://www.quimicaorganica.org/estereoquimica/86-clasificacion-de-isomeros.html |
 |
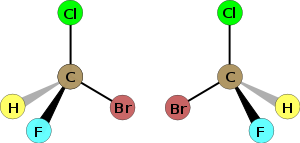
| AMBOS DE FÓRMULA MOLECULAR C5H12O. SON ISÓMEROS DE POSICIÓN. fuente: http://www.quimicaorganica.org/estereoquimica/86-clasificacion-de-isomeros.html |
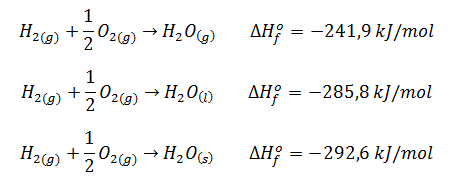 |
| Fuente: https://www.google.es/search?q=ecuaci%C3%B3n+termoqu%C3%ADmica&biw=1280&bih=699&source= lnms&tbm=isch&sa=X&ved=0ahUKEwiZtJTlk4TLAhVDPRoKHamCAjMQ_AUIBygC&dpr=1#tbm= isch&q=ecuaci%C3%B3n+termoqu%C3%ADmica+formacion+h20+en+color&imgrc=oHZxMunnzT_0nM%3A LAS TRES REACCIONES DE FORMACIÓN DE AGUA EN DISTINTOS ESTADOS FÍSICOS SON EXOTÉRMICAS (liberan energía) |


 |
| http://www.andritzgouda.com/es/index.php/proceslijn/Starch_dextrination |

